所有生命科學產業廠商正被其所在地的政府機關,強制要求得遵循相關於作業流程的品質規範,這些法規明訂了一項產品從生產、銷售到行銷推廣各層面的嚴格規定。若違反相關規定便得接受相當程度的罰鍰和被要求進行產品回收。
QAD 與生命科學行業
QAD的ERP解決方案提供了生命科學和醫療器材行業製造商所需的靈活性。

對生命科學行業的承諾和願景
生命科學和醫療器材製造航商致力於創新、產品品質和患者安全,但是監管環境越來越嚴格、成本壓力增大以及供應鏈的複雜性帶來了新的挑戰。新興的全球市場、品質計劃以及併購活動的日益加劇,增加了醫藥或醫療器材生產和銷售的複雜性。QAD的ERP解決方案提供了生命科學行業製造商所需的靈活性。

生命科學行業特色及專屬需求
醫藥和醫療器材製造商致力於創新、產品質量和患者安全,
但是監管環境越來越嚴格、成本壓力增大以及供應鏈的複雜性帶來了新的挑戰。
行業特色及趨勢
全球生命科學行業仍在經歷著巨大的變化。該行業製造商繼續致力於不斷研發創新,提高產品品質,加強對患者的安全保障,但如今製造商面臨的法規遵循、成本和醫療理賠壓力比以往任何時候都要大。
面對生命科學行業供應鏈的全球化發展趨勢,其中新頒布的《Drug Quality and Security Act藥品品質與安全法案》和醫療器材單一識別系統(UDI) 等新法規的要求,以及妥善管理產品召回和假冒藥品問題等情況,讓生命科學行業製造商如何維持領導地位變得更加複雜。

參考文章:藥品供應鏈安全法案(The Drug Supply Chain Security Act, DSCSA)介紹:您準備好了嗎?
參考文章:如何在即將實施的歐盟醫療器材和體外診斷醫療器材(iVD)法規中茁壯成長
生命科學行業垂直細分市場及其特色
QAD 致力於向製造企業提供以行業為中心的高品質ERP軟體,
為了幫助您的業務提升到一個新的水平,我們專注於每個行業的垂直細分市場。
生命科學委託生產服務
生命科學委託生產服務商為製藥和醫療器械公司提供製造、包裝和其他合同服務。
他們面臨競爭激烈並需要更高運營效率的分散市場,需要更高的運營效率,並關注關鍵指標,如庫存減少、產能利用率和改進的客戶服務指標。
體外診斷(IVD)製造商
IVD公司生產用於疾病篩查、診斷和監測的試劑和儀器。
IVD製造商面臨的挑戰是生產創新的檢測方法並跟上快速變化的臨床趨勢,同時繼續專注於開發優化檢測效率和患者結果的新解決方案。
醫療器材
醫療器材製造商生產專門設計的設備或套件,用於執行醫療領域的特定手術。
隨著監管的加強,競爭的激烈和報銷的減少,醫療設備公司正被驅使改善病人和醫療設施的重點指標。
製藥和生物技術
製藥和生物技術公司研發和製造用於治療和控制疾病以及保護免受感染的藥物。
他們面臨著一個由嚴格的法規和複雜的供應鏈管理的競爭性全球市場,並尋求將品質納入其核心業務流程和供應鏈規劃的方法。
專為化學製藥、生技業和醫療器材製造業打造ERP解決方案
QAD承諾發展最新的解決方案來配合產業最新的需求,
而產品都是QAD和其生命科學業的客戶、合作夥伴和全球產業協會所共同發展的成果。
主要面對的挑戰和機會
全球產業
規範遵循
新產品的
市場推廣
QAD提供各工具,來管理從研發、生產到行銷推廣各階段中相關資源管理和成本控管等作業。QAD解決方案將可使您在生產製造面獲得最大效能,並可讓您在銷售通路上更具獲利性。
降低風險
生命科學產業業者負有嚴格的使命,得確實維持系統的安全性和可稽核性。
從研發到生產階段,相關細節涵蓋:一個產品如何被製成?以及其可被分析及控管的組成原料為何?都得被嚴格的要求和驗證。
QAD 提供生命科學產業製造業一套工具,能讓其具備管理相關確效驗證(Validation)、電子簽章和記錄、完整的稽核軌跡(Audit Trails)和批次追溯能力(Lot Traceability)來降低相關風險和以有成本效益的方式來管理法規遵循業務。
QAD可滿足您行業的關鍵需求
生命科學產業客戶眾多經營管理面的關鍵需求
QAD解決方案提供行業專屬功能
(Enhanced Controls)


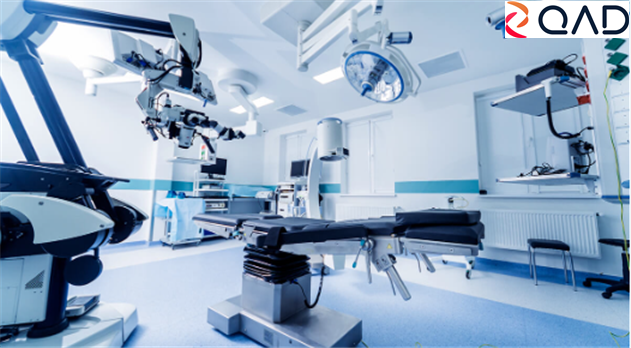
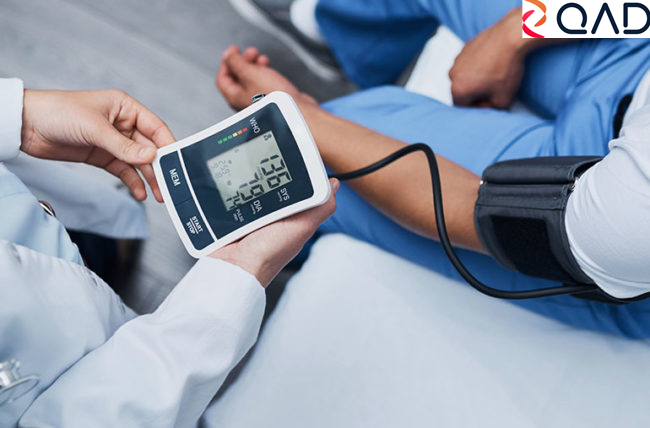
QAD與體外診斷設備行業
QAD 提供整合的ERP應用程式組合,可支持體外診斷設備生産商不同的計劃和生産需求。針對性解决方案包括企業範圍品質合規管理(EQMS)、倉儲、需求和供應鏈計劃以及生産車間可視化等。

台灣知名醫療器材供應商舉辦QAD ERP升級專案布達會議
該公司目前使用多年前導入的舊版本QAD ERP,這幾年來體認老舊的ERP已無法滿足集團業務發展及作業需求,惟有QAD系統升級才能滿足來自客戶各樣的需求及解決諸多作業瓶頸。

欣眾科技宣佈與國內備受矚目的生技製藥公司合作,協助導入QAD ERP系統
在充份了解QAD可提供生技製造業完整ERP解決方案及滿足國內外營運據點所需的財務合規功能,以及欣眾科技多年來深耕生命科學行業所累積的眾多客戶及系統實施經驗。最後選擇QAD及欣眾科技做為ERP實施合作夥伴。

安成藥業因應商業高度競爭,建立一套醫療生技產業專屬、可滿足現今和未來產業需求的ERP平台
我們的QAD專案進行的非常順利,我們非常感謝欣眾公司的協助,QAD ERP是一個非常好的選擇,它提供的解決方案適合醫藥產業特性和需求。
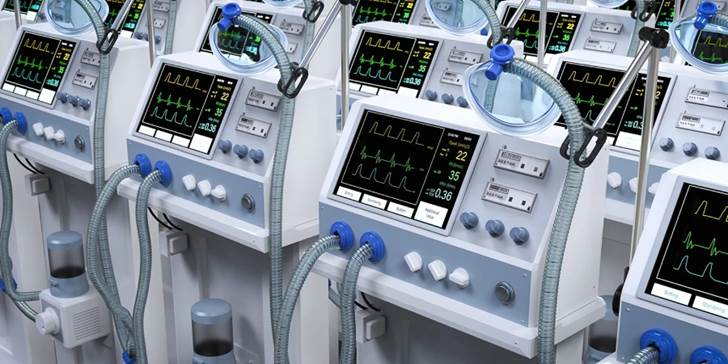
符合歐盟MDR規範:醫療器材製造商的關鍵期限
2024年9月26日,對於在歐盟地區銷售醫療器材的生命科學公司而言,是一個關鍵的期限。在此日期之前,醫療器材製造商必須與其第三方驗證機構(notified bodies)合作,以確保其醫療器材的合規認證能夠展延並符合歐盟醫療器材法規:EU MDR 2017/745。

符合全球UDI規範:對病患和醫療器材製造商有利
美國食品藥物管理局(FDA)的目標是透過通用醫療器材單一識別系統(Universal Device Identification system),提高醫療器材在整個生命週期的可追蹤性,以保障病患和臨床醫師使用者的安全。

QAD Adaptive ERP統一了Noble Biomaterial公司的業務流程
我們選擇QAD Adaptive ERP的原因之一是擁有一個真相版本的重要性。我們以前有資料,但各利益相關方無法就什麼是準確的資料達成一致共識,因為它的來源非常多。

知名營養補充劑公司Vit-Best 選擇基於雲端的QAD Adaptive ERP
Vit-Best公司在一個高度監管的行業中競爭,在遵守我們服務的所有國家的監管規定的同時,超越客戶期望的能力至關重要。QAD Adaptive ERP將為我們提供一個易於擴展的平台。
QAD ERP 系統幫助管理嚴格的製藥公司Ajinomoto Althea提升 cGMP 實踐能力
Althea 專門成立了一個 ERP 評估小組,根據預先定義的挑選標準清單,對20多種不同的ERP系統進行了審核。經過對比,Althea 最終敲定 QAD的ERP系統。
IMRS利用QAD企業平台及QAD ADAPTIVE UX減少了記錄服務電話的時間,減少了點擊完成鍵的次數
使用者的工作效率更高,作業流程可以更少的點擊和更少的時間來完成,而且公司的所有系統客制都有完整的記錄檔。
Laerdal - QAD生命科學業客戶成功案例
Laerdal是一家為全球醫療保健提供商,志願組織,教育機構,醫院和軍隊開發產品和計劃的公司。Laerdal在24個國家...
Sharp Corporation - QAD生命科學業客戶成功案例
使用QAD序列化解決方案,在整個全球供應鏈中提供醫藥產品的跟蹤和追溯能力。...